黄斑变性治疗医学研究
临床实验的治疗年龄相关性黄斑变性(AMD)是在不同开发阶段的治疗但尚未被FDA批准用于美国,尽管他们可能在其他国家。
在某些情况下,美国人可以接收这些疗法之前,FDA批准,特别是如果他们参加临床试验这有助于确定药物的安全性和有效性,手术或其他治疗。
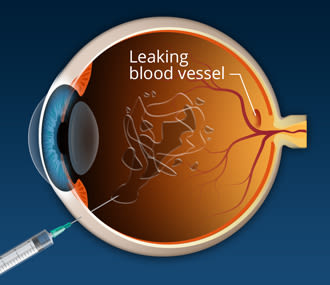
大多数临床实验的治疗方法正在开发治疗黄斑变性目标更高级和视觉毁灭性的“湿”形式的疾病,表现为异常的形成,血管渗漏在中央视网膜。
然而,一些研究人员正在试图找到一个有效的治疗更为常见的“干”AMD视觉的影响还不算严重。
黄斑变性的治疗
Eylea和抗体联合治疗。Regeneron是美国的制药公司Eylea——一个建立,fda批准医学治疗湿性AMD。Eylea是一个抗vegf(血管内皮生长因子)药物注入眼睛缓慢,停止或逆转漏水的视网膜中央血管的形成。
2016年9月,Regeneron发布的2期临床试验结果Eylea联合治疗,rinucumab(一种特定类型的抗体称为anti-PDGFR-beta)是为了看看这个组合将增强治疗湿性AMD的好处Eylea孤单。
不幸的是,Eylea /抗体联合治疗不展示最佳矫正的改善视敏度(BCVA),而独自Eylea治疗12周后,这是这项研究的主要终点。病人在两个联合治疗组显示5.8信改善BCVA标准视力表,而患者Eylea仅显示7.5信改进。同时,联合治疗组患者经历更多的副作用,包括结膜下出血、眼睛刺激和眼睛疼痛。
在第12周,两三个治疗组在研究的第一阶段是re-randomized,导致五总剂量组的第二阶段研究。结果这些团体将在28周评估,再次在52周,当这项研究完成后,根据该公司。
Regeneron也进行组合研究Eylea (aflibercept)和不同类型的抗体称为nesvacumab,更支持的临床前数据,根据乔治·d·Yancopoulos,医学博士,博士公司的首席科学官和总统Regeneron实验室。这种联合治疗的研究结果尚未公布。
阿瓦斯丁。一些眼科医生使用阿瓦斯丁(贝伐单抗),fda批准的癌症药物由Genentech时,作为一个“标签”治疗黄斑变性。
“标签”使用意味着阿瓦斯丁没有专门fda批准的黄斑变性的药物。尽管Genentech市场阿瓦斯丁用于治疗直肠癌,该公司已宣布不打算把药物临床试验治疗黄斑变性。
当使用标签将AMD,阿瓦斯丁是直接注射到玻璃的后面眼睛,就像Lucentis——fda批准的药物也由Genentech黄斑变性。
在一项研究中被称为年龄相关性黄斑变性治疗的比较试验(土)由美国国家眼科研究所比较的有效性阿瓦斯丁和Lucentis治疗湿性AMD,阿瓦斯丁被发现Lucentis相当于在类似的给药方案。在所有治疗组在这项研究中,至少有60%的患者达到视力达到或超过法定标准驾驶视野(20/40或更好)。
一些眼部护理从业人员选择使用阿瓦斯汀标签AMD治疗,因为病人成本可以明显低于使用Lucentis时,获得FDA批准为黄斑变性治疗2006年。
其他眼科医生说Lucentis应该首选的治疗方法,尽管它是更昂贵的,因为药物经历了临床试验和可核查的结果具体治疗黄斑变性。
ohr - 102。这是一个正在开发的临床实验的辅助治疗湿性AMD Ohr制药。
2015年11月,该公司宣布的第二阶段研究结果评价结合ohr - 102滴眼剂的效果与Lucentis注射药物治疗湿性AMD患者。在早期的湿性AMD患者,40%的患者的组合ohr - 102 + Lucentis的获得3或更多行最佳矫正视力,相比之下,26%的病人只有Lucentis治疗(54%的额外的好处)。
Ohr制药目前正在进行第三阶段的研究Ohr - 102和Lucentis联合治疗在更大的组患者证实其有效性。
mc - 1101。正在开发的早期研究表明这个临床实验的AMD MacuCLEAR可能有助于防止干AMD发展到湿性AMD通过增加血液流动脉络膜血管的薄层夹在了巩膜和滋养视网膜的视网膜。
MacuCLEAR在2012年宣布它已收到资金从目前投资者完成第三阶段测试的药物治疗和进入战略伙伴关系与环太平洋制药公司和投资者为临床成本,桥接研究和监管发展mc - 1101在这一地区。
药物植入物
初PDS。基因泰克是追求重复使用港口的发展输送系统(PDS)植入的眼睛。设备包含之初,同样的药物用于公司的注射Lucentis。
的first-in-human结果植入了2012年在美国眼科学会的和未来的研究计划,以帮助确定剂量和推荐的续杯之间的时间长度。
Renexus (nt - 501)。Neurotech制药宣布了有前景的结果的临床研究nt - 501眼内植入治疗色素性视网膜炎。
植入包含转基因人类细胞能够分泌神经生长因子能够拯救和保护死亡光感受器在视网膜上。该公司表示,治疗也可能有效的治疗黄斑变性。共有184名受试者已经进入了三个独立的第二阶段研究在美国
人工视网膜
研究越来越成为专注于发展人造视网膜或刺激视网膜的方法对于那些经历了从视网膜疾病永久性视力丧失。为例,视力仿生学是研究人造硅视网膜(ASR)芯片作为一种刺激健康的视网膜细胞恢复视力对于那些色素性视网膜炎等疾病,黄斑变性。
基因治疗
研究基因治疗作为一种潜在的治疗黄斑变性是在早期阶段。但是调查人员正在寻找方法引入特殊编码的基因可能会改变过程导致黄斑变性。
干细胞
在什么可能是治疗干性AMD的一个里程碑,2015年6月,Ocata疗法提出了四个前瞻性试验调查结果使用视网膜色素上皮(RPE)细胞来自人类胚胎干细胞治疗黄斑变性病和干燥的黄斑变性。
黄斑变性病(也称为黄斑变性黄斑营养不良)是一种视网膜黄斑变性影响年轻人。它会影响估计有80000到100000人在美国和欧洲,并导致进步的视力丧失,通常10到20岁之间的开始。
所有31个病人参与试验经验改善或稳定的最佳矫正视力(BCVA)。
2016年2月,Ocata疗法被日本的阿斯特拉制药公司收购,并在2016年5月,更名为阿斯特拉再生医学研究所(AIRM)。总部设在马萨诸塞州马尔伯勒AIRM间接,阿斯特拉的全资子公司,作为公司的再生医学和细胞疗法研究全球中心眼科和其它治疗领域很少或根本没有可用的治疗方案,根据阿斯特拉。
2015年6月,另一家公司,干细胞的公司。有利的结果的宣布,1/2期临床试验的安全性和初步效果评估公司的净化人类神经干细胞治疗干性AMD。
基于这些研究的力量,公司启动了二期研究被称为辐射研究。然而,进一步招生已经暂停,而公司寻求资金的合作伙伴,根据该公司的网站。
请点击这里阅读fda批准的黄斑变性的治疗。
与rinucumab Regeneron宣布的第二阶段研究aflibercept co-formulated (anti-PDGFR-beta)显示没有好处aflibercept新生血管性年龄相关性黄斑变性。2016年9月发布的新闻稿Regeneron药品。从Ohr Ohr制药带来了新的数据- 102二期影响研究在湿性amd在美国眼科学会的年度会议。2015年11月发布的新闻稿Ohr制药。之初,贝伐单抗治疗新生血管性年龄相关性黄斑变性:两年的结果。眼科学。2012年7月。阿瓦斯丁治疗年龄相关性黄斑变性和Lucentis是等价的。国家眼科研究所。2012年4月。
周三发布页,2019年2月27日
页面更新周二,2022年3月15日